Biotechnologies
La révolution de la biofonderie : programmer la vie comme une usine

Le passage des usines chimiques aux usines biologiques
Comment le code numérique remplace les produits chimiques de synthèse
Dès que les premiers scientifiques ont compris que le monde matériel qui les entourait était composé d'éléments purs et distincts, ils se sont efforcés de mieux le comprendre. Les travaux des premiers alchimistes ont ouvert la voie aux scientifiques du siècle des Lumières et au début de l'époque moderne, lorsqu'ils ont découvert les éléments et les fondements de la biologie : les cellules, l'ADN, etc.
Dans le même temps, l'industrie chimique créait les prémices de l'industrie pharmaceutique, utilisant des médicaments chimiques de synthèse pour modifier les processus biologiques chez les patients, comme l'utilisation de l'acide salicylique (aspirine) pour faire baisser la fièvre.
Les produits chimiques utilisés en médecine et dans l'industrie sont progressivement devenus de plus en plus complexes. Or, plus une molécule est complexe, plus sa synthèse par des méthodes chimiques artificielles est difficile. Elle devient même impossible pour les protéines ou les composés biochimiques les plus complexes.
Ensuite, le génie biologique a permis la production, par des microbes OGM, d'insuline, d'hormones de croissance, d'anticorps, etc., à la fois bon marché et sûrs, créant ainsi le domaine de la biotechnologie comme un domaine connexe, mais distinct, de l'industrie pharmaceutique.
Ce fut une révolution majeure en biochimie et en médecine, rendant soudainement abondants et bon marché la production de composés qui étaient auparavant extrêmement coûteux, voire impossibles à obtenir.
Aujourd'hui, de nombreuses nouvelles technologies (mégadonnées, IA, automatisation, ingénierie génétique de précision, analyses avancées, etc.) convergent pour ouvrir une nouvelle ère des biosciences : la révolution des biofonderies.
Au-delà de la nature : repenser les organismes pour l'industrie
L'ère des biotechnologies a été marquée par l'utilisation de modifications génétiques artificielles pour amener des micro-organismes à produire des biomolécules d'intérêt, généralement des produits médicaux. Cette approche s'est avérée extrêmement rentable, car nombre de ces molécules sont soit des produits vitaux, soit des produits à haute valeur ajoutée qui, auparavant, ne pouvaient être obtenus qu'en petites quantités par des méthodes onéreuses.
Cependant, cette méthode présente la limite intrinsèque de ne pouvoir reproduire que ce qui existe déjà dans les organismes vivants. Or, à ce jour, la production de nombreux matériaux et molécules utiles repose sur des produits chimiques synthétisés artificiellement, par des procédés toxiques ou émetteurs de carbone.
Ainsi, bien que la transformation de notre système énergétique par le biais des véhicules électriques, des batteries et des énergies renouvelables soit importante, la recherche d'alternatives plus écologiques à la production chimique est tout aussi importante pour résoudre la plupart des problèmes du monde moderne : pollution plastique, changement climatique, agriculture durable, production industrielle non polluante, biosécurité, maladies incurables, médecine régénérative, traitements de longévité, etc.
Et à tous ces problèmes, une solution est désormais mise en œuvre : le modèle de la biofonderie.
Comment fonctionne le modèle de la biofonderie : une convergence technologique
Multiomique, CRISPR et l’essor du « bio-codage »
Ces dernières années, la compréhension de la biologie et de la génétique a fait des progrès considérables. Ces progrès reposent en grande partie sur quelques technologies novatrices.
La première est le séquençage et la génomique, qui sont devenus suffisamment bon marché pour être réalisés de manière routinière pour moins de 1 000 dollars par organisme.
Elle est désormais combinée à de nombreuses autres approches « -omiques » (transcriptomique, protéomique, métabolomique, épigénomique, microbiomique, biologie spatiale) pour créer multiomique, une compréhension holistique de tous les multiples niveaux de complexité des organismes vivants.
Une autre technologie novatrice est CRISPR, une nouvelle méthode d'édition génétique découverte en 2012, qui est depuis devenue la méthode la plus puissante pour modifier les gènes de tous types d'organismes, y compris pour guérir des maladies rares.
Enfin, l'émergence du big data, de l'IA et d'autres formes d'analyse avancée a donné aux biologistes les outils nécessaires pour traiter et donner un sens au déluge de données généré par la multiomique.
Leur combinaison fait émerger une toute nouvelle capacité.
La combinaison de tonnes de données issues de la multiomique biologique réelle avec l'analyse par IA signifie que l'ensemble du processus de création de molécules complexes peut être cartographié, modélisé et même entièrement simulé. in silicoCela ouvre la possibilité de tester des milliers de possibilités ou de créer de toutes pièces des protéines entièrement nouvelles dotées de propriétés inédites.
Et grâce à CRISPR, intégrer ces idées dans de véritables micro-organismes ou plantes n'a jamais été aussi rapide, précis et facile, les transformant en usines biologiques bien contrôlées, ou « biofonderies », une sous-section de la biologie synthétique.
L'ADN étant essentiellement un code biologique, la facilité de production d'OGM et de conception de nouveaux biosystèmes rapproche la biologie de la programmation informatique.
« Imaginez une cellule. C'est une sorte de petite machine qui fonctionne grâce à un code numérique, très similaire à un ordinateur, sauf qu'ici, au lieu de zéros et de uns, ce code est composé de A, de T, de C et de G. La biologie synthétique consiste donc à programmer les cellules comme on programme les ordinateurs, en modifiant leur code ADN. Nous sommes en quelque sorte des programmeurs cellulaires à notre service. Notre travail consiste à faire en sorte que la cellule agisse selon les souhaits de nos clients. »
Jason Kelly – PDG de Ginkgo Bioworks
Du plastique au parfum : ce que les biofonderies peuvent construire
De nombreux produits chimiques actuellement fabriqués par l'industrie chimique pourraient, en théorie, être remplacés par des produits biologiques. Soit par la même molécule produite par des organismes vivants, soit par des substituts aux propriétés similaires.
Par exemple, les micro-organismes du sol et les plantes produisent naturellement, en petites quantités, des engrais, de l'éthanol ou de l'éthylène, autant de molécules actuellement produites en masse par l'industrie chimique. Ainsi, un rendement supérieur ou une production moins coûteuse par un organisme vivant pourrait avoir un impact carbone bien moindre.
Un autre objectif est de réduire la dépendance aux combustibles fossiles en produisant des polymères, notamment des textiles et des plastiques (1,4-butanediol, 1,3-propanediol, polyhydroxyalcanoates, polylactique, etc.) par des voies métaboliques biologiques.
Les parfums de grande valeur, les acides aminés, les vitamines, la soie, les arômes comme la vanilline et les ingrédients cosmétiques comme le squalane ou l'acide hyaluronique pourraient tous être produits en masse naturellement et à faible coût, du moins en théorie.
Et bien sûr, de nombreuses molécules biologiques nouvellement inventées peuvent servir à la fabrication de vaccins synthétiques, de traitements anticancéreux, de sources alternatives de protéines et d'aliments (viande cultivée, etc.).
Enfin, cette méthode permet de fabriquer des produits entièrement nouveaux. Par exemple, le mycélium de champignons peut constituer une alternative viable au cuir et à d'autres textiles. De même, les émissions de carbone peuvent être directement recyclées en produits utiles avant même d'atteindre l'atmosphère.
Le modèle commercial de la recherche en tant que service
Créer des synergies
Si la technologie permettant de le faire a atteint sa maturité, il n'est cependant pas si simple en pratique de réécrire entièrement le métabolisme d'un être vivant, tout en maintenant sa productivité.
C’est pourquoi l’externalisation de cette tâche auprès d’entreprises spécialisées, disposant des équipements, de l’expertise et du matériel biologique adéquat, est une tendance croissante. Ce modèle de « recherche à la demande », également appelé « organismes à la demande », permet à différents projets et concepts de se soutenir mutuellement dans divers domaines.
Par exemple, un micro-organisme initialement conçu pour absorber les émissions de carbone peut également utiliser ce carbone pour produire de l'éthylène, un précurseur essentiel à de nombreuses réactions de synthèse chimique. Cependant, une entreprise spécialisée dans les crédits carbone n'aurait ni utilisation immédiate ni expérience de l'éthylène, tandis qu'une entreprise chimique pourrait ne pas disposer d'une source de carbone à proximité. En revanche, en faisant appel au même prestataire de biofonderie, les deux entreprises peuvent développer des synergies et optimiser le processus.
De même, une nouvelle méthode optimisée de modifications génétiques peut être déployée pour des dizaines d'applications différentes, amortissant ainsi les coûts de R&D sur un plus large éventail de projets.
Ginkgo Bioworks : L’« ADN » de la biologie synthétique
Aucune entreprise n'a été plus à l'avant-garde du développement des « organismes à la demande » que Ginkgo Bioworks. Fondée en 2008 par cinq scientifiques du MIT, l'entreprise s'est consacrée à la production de bactéries OGM pour des applications industrielles, la biotechnologie, généralement au cœur de ce type d'activité, n'étant qu'une préoccupation secondaire.
Ginkgo a été la première entreprise de biotechnologie à rejoindre le célèbre programme d'accélération de start-up Y Combinator en 2014. L'entreprise est entrée en bourse en 2021 par le biais d'une fusion avec une SPAC et a réussi à obtenir le symbole boursier NYSE DNA, précédemment détenu par le pionnier de la biotechnologie Genentech (avant son acquisition par Roche).
Ginkgo Bioworks Holdings, Inc. (DNA -7.49%)
Depuis, Gingko Bioworks est devenu un partenaire clé de nombreuses entreprises industrielles, pharmaceutiques et agricoles.

Source: Gingko Bioworks
Par exemple, elle a développé de nouveaux organismes pour divers programmes de recherche :
- Des microbes programmables pour les maladies intestinales.
- Bioremédiation des microplastiques.
- Thérapies et vaccins à ARN.
- Recyclage des déchets et des contaminants.
- Maîtriser les maladies critiques du soja au Brésil.
- Remplacer les engrais azotés par des bactéries
- Cannabinoïdes.
- Fabrication optimisée de produits biologiques et de peptides
- Production de principes actifs pharmaceutiques (API) par biocatalyse et fermentation à grande échelle.
- Solutions de diagnostic moléculaire, grâce à une base de données enzymatiques exclusive et à des concepteurs d'enzymes experts.
- Thérapie cellulaire et édition génique.
Le virage stratégique de Gingko : vendre la biosécurité aux laboratoires autonomes
Vente de l'entreprise de biosécurité
Durant la pandémie de COVID-19, Gingko a rapidement développé son activité de biosécurité, qui consiste à surveiller les risques biologiques, principalement pour les gouvernements. Cette activité a ensuite évolué vers une plateforme de bioradar complète.
Cette activité a apporté une contribution inestimable pendant la pandémie grâce à nos programmes de dépistage nationaux et régionaux, et a généré un chiffre d'affaires annuel record de plus de 300 millions de dollars. Nous sommes fiers d'avoir contribué à la réouverture de plus de 5 000 écoles à travers le pays.
Cependant, cette activité est relativement indépendante des autres projets de Gingko Bioworks. La direction a donc décidé de la céder à un consortium d'investisseurs, créant ainsi une nouvelle entité privée indépendante nommée Tower Biosecurity. Gingko conservera néanmoins une participation de 20 %.
Du statut de prestataire de services à celui de partenaire à forte valeur ajoutée
L'activité « organismes à la demande » constitue actuellement le cœur de métier de l'entreprise, les principaux segments étant l'agroalimentaire et l'industrie pharmaceutique et biotechnologique. Cependant, son chiffre d'affaires a diminué entre le quatrième trimestre 2024 et le quatrième trimestre 2025, en raison d'un recul général des investissements en biotechnologie durant cette période.

Source: Gingko Bioworks
Ce segment a souffert d'une relative incertitude quant à son modèle économique. Initialement, Gingko prévoyait de proposer uniquement des services de recherche, à prix fixe et avec une échéance clairement définie. Cette approche a contribué à la grande popularité de Gingko en tant que partenaire de recherche.
Cependant, cela signifiait aussi qu'il n'y avait pas de redevances résiduelles ni de revenus supplémentaires une fois le projet terminé, ce qui signifiait que Gingko était coincé dans un cycle sans fin de nouveaux projets, la prouesse technologique ne se traduisant pas vraiment en revenus.
Depuis, elle a commencé à développer de nouveaux organismes davantage axés sur une structure de partenariat. Par exemple, la réalisation d'une étape majeure dans un projet avec Merck, menant à un versement de 9 millions de dollars au quatrième trimestre 2024 et des paiements plus importants ultérieurement, lors de la deuxième phase du projet.
L'entreprise a pris au sérieux la nécessité de se restructurer pour améliorer sa trésorerie, et a déployé des efforts considérables pour réduire sa consommation de trésorerie, qui a diminué de 73 % au cours de l'année écoulée. Par ailleurs, elle ne présente aucune dette significative, ce qui limite davantage ses risques financiers.

Source: Gingko Bioworks
L'essor du laboratoire de robotique modulaire et autonome
Si l'ingénierie cellulaire a longtemps été au cœur de l'activité de l'entreprise, son avenir repose désormais sur l'utilisation de l'IA et de ses propres laboratoires automatisés pour réduire les coûts et améliorer la création de nouvelles biofonderies.
Laboratoires automatisés Il s'agit d'une technologie sur laquelle Gingko travaille depuis un certain temps, car aujourd'hui encore, la plupart des tâches dans les laboratoires de biologie sont des tâches manuelles répétitives et fastidieuses, qui consomment souvent la majeure partie du temps d'une main-d'œuvre titulaire de maîtrises et de doctorats.
Pour changer cette méthode, elle a créé une plateforme modulaire automatisée, capable d'effectuer sans intervention humaine des tâches de laboratoire telles que la culture de cellules, le transfert de produits chimiques, l'analyse microscopique, etc.

Source: Gingko Bioworks
La principale caractéristique de cette conception est sa modularité. Chaque élément peut ainsi être connecté à un autre afin de créer une sorte de « chaîne d'assemblage » pour les expériences scientifiques et les bioanalyses.
Cette solution est combinée à une offre logicielle, créant une solution flexible qui peut être adaptée et modifiée en quelques jours ou quelques heures seulement, par rapport aux infrastructures de recherche plus rigides nécessitant des mois de reconfiguration coûteuse pour les nouveaux projets.

Source: Gingko Bioworks
Cette combinaison offre à la fois la flexibilité nécessaire à la recherche (par rapport à la production de masse), mais aussi l'automatisation nécessaire pour accélérer la recherche et réduire les coûts, car le laboratoire automatisé peut travailler plus rapidement qu'un humain et 24 heures sur 24, 7 jours sur 7.
Gingko prévoit de proposer cette technologie sous deux formats :
- « Construisez votre propre laboratoire », où l'entreprise fabrique et entretient les modules de laboratoire automatisés, mais la gestion quotidienne et la propriété appartiennent au client.
- Accédez au laboratoire autonome de pointe de Ginkgo en souscrivant directement au service.
Point de données : Générer 10 000 expériences en quelques semaines
Tandis que la solution d'automatisation génère les données biologiques, Datapoint les traite pour en tirer des informations utiles.
L’élément clé est la génération rapide de données qui peuvent guider d’autres hypothèses et l’itération rapide de nouvelles expériences pour continuer à avancer.
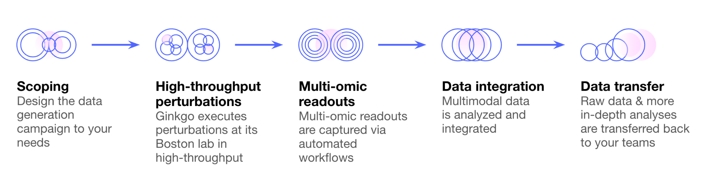
Source: Ginkgo Bioworks
Grâce à ce service, Ginkgo peut fournir des données appartenant intégralement au client, ce qui constitue un avantage concurrentiel dans le cadre de partenariats avec d'autres entreprises de biotechnologie ou pharmaceutiques.
Les données peuvent être générées en seulement 3 semaines, avec plus de 10 000 perturbations chimiques et génétiques in vitro dans chaque type cellulaire, et un large choix de méthodes analytiques disponibles pour étudier les résultats.
Le même système peut être utilisé pour la génération rapide de nouveaux anticorps, un type de molécule devenant rapidement un médicament clé en oncologie et dans d'autres domaines médicaux. Ginkgo peut analyser jusqu'à 2,400 1 anticorps différents en parallèle, grâce à une infrastructure de laboratoire automatisée d'une valeur d'un milliard de dollars.
Recherche biologique basée sur l'IA
Gingko a établi un partenariat avec OpenAI pour utiliser ChatGPT 5 dans le cadre de la recherche biologique. L'entreprise a constaté une nette amélioration de sa productivité.
« La société indique que le système a permis de réduire de 40 % les coûts des réactions de synthèse protéique acellulaire par rapport aux méthodes de pointe, tout en exécutant 36 000 conditions expérimentales sur six cycles itératifs. »
L'intervention humaine se limitait principalement à la préparation, au chargement et au déchargement des réactifs, ainsi qu'à la supervision du système, tandis que la conception expérimentale, l'exécution, l'interprétation des données et la formulation des hypothèses étaient gérées par le laboratoire autonome piloté par GPT-5.
Le modèle utilisé a été publié en tant que code source ouvert, et Le mélange réactionnel acellulaire amélioré par l'IA peut être commandé par la communauté scientifique., faisant du ginkgo un outil de recherche open source important pour les scientifiques du monde entier.
Ginkgo était également 47 millions de dollars accordés par le gouvernement américain pour le développement d'un grand centre de recherche pour le Mission Genesis, un site de 32 000 pieds carrés connu sous le nom de Capacité de phénotypage moléculaire microbien (M2PC)Il abritera plus de 100 instruments d'analyse automatisés et devrait être pleinement opérationnel pour les chercheurs du monde entier d'ici 2030.
« L'équipe exploitera l'IA avancée pour décrypter la fonction des protéines et des voies métaboliques, automatiser la génération et la collecte de données et intégrer les systèmes expérimentaux et de supercalcul du DOE aux entreprises de biotechnologie et d'IA. »
Perspectives à long terme : le ginkgo est-il enfin rentable ?
Créateur du modèle commercial de la biofonderie et acteur majeur de la biosécurité, Gingko se réinvente aujourd'hui en tant que leader de l'automatisation de la recherche biologique et partenaire clé des technologies de R&D pilotées par l'IA.
À la croisée de la biologie et de l'intelligence artificielle, de nombreux procédés industriels seront progressivement remplacés par des bioprocédés plus écologiques, neutres en carbone, non toxiques et moins coûteux. Dans cette vision du futur, les formes de vie sont aussi programmables que le code informatique, mais leur impact sur le monde réel est encore plus important.
Cela représente une formidable opportunité pour Gingko Bioworks, que ce soit pour le projet sur lequel elle travaille déjà, ou pour que sa conception de laboratoire automatisé devienne à long terme la norme pour la plupart des équipes de recherche.
Conjuguée à une amélioration de son modèle commercial d'ingénierie cellulaire (avec des redevances plus élevées et des contrats de partage des revenus plus équitables), cette mesure devrait contribuer à rendre Gingko rentable dans les années à venir.
(Vous pouvez également en savoir plus sur d'autres entreprises de biologie synthétique dans «Top 5 des sociétés publiques de biologie synthétique»)











