BioTech
La revolución de la biofundición: programar la vida como una fábrica.

El cambio de la química a las fábricas biológicas
Cómo el código digital está reemplazando a los productos químicos sintéticos
En cuanto los primeros científicos comprendieron que el mundo material que los rodeaba estaba compuesto de elementos puros e independientes, comenzaron a trabajar para comprenderlo mejor. El esfuerzo de los primeros alquimistas allanó el camino para los científicos de la Ilustración y la primera época moderna, cuando descubrieron los elementos individuales y los fundamentos de la biología: las células, el ADN, etc.
Al mismo tiempo, la industria química estaba creando la incipiente industria farmacéutica, utilizando fármacos químicos sintéticos para alterar los procesos biológicos en los pacientes, como el uso del ácido salicílico (aspirina) para bajar la fiebre.
Progresivamente, los productos químicos utilizados en medicina e industria se volvieron cada vez más complejos. Sin embargo, en gran medida, cuanto más compleja es una molécula, más difícil resulta sintetizarla mediante métodos químicos artificiales. Y se vuelve prácticamente imposible para las proteínas o compuestos bioquímicos más complejos.
Posteriormente, la bioingeniería permitió la producción, mediante microorganismos transgénicos, de insulina, hormona del crecimiento, anticuerpos, etc., baratos y seguros, creando así el campo de la biotecnología como un campo relacionado, pero distinto, del farmacéutico.
Esto supuso una revolución enorme en la bioquímica y la medicina, ya que de repente se hicieron abundantes y baratos compuestos que antes eran extremadamente caros o imposibles de obtener.
Hoy en día, muchas tecnologías nuevas (macrodatos, inteligencia artificial, automatización, ingeniería genética de precisión, análisis avanzados, etc.) están convergiendo para abrir una nueva era de las biociencias: la revolución de la biofundición.
Más allá de la naturaleza: rediseñando organismos para la industria.
La era de la biotecnología se caracterizó por el uso de modificaciones genéticas artificiales para lograr que los microorganismos produjeran biomoléculas de interés, generalmente productos médicos. Esto ha resultado extraordinariamente rentable, ya que muchas de estas moléculas son productos que salvan vidas o de alto valor que anteriormente solo podían obtenerse en pequeñas cantidades mediante métodos costosos.
Sin embargo, esto tiene la limitación inherente de que solo puede replicar lo que ya existe en los organismos vivos. Pero hasta el día de hoy, la producción de muchos materiales y moléculas útiles depende de productos químicos producidos artificialmente, utilizando métodos tóxicos o que emiten carbono.
Si bien es importante transformar nuestro sistema energético mediante vehículos eléctricos, baterías y energías renovables, encontrar alternativas más ecológicas a la producción química es igualmente importante para resolver la mayoría de los problemas del mundo moderno: la contaminación por plásticos, el cambio climático, la agricultura sostenible, la producción industrial no contaminante, la bioseguridad, las enfermedades incurables, la medicina regenerativa, los tratamientos para prolongar la vida, etc.
Y para todos estos problemas, ahora se está implementando una solución: el modelo de biofundición.
Cómo funciona el modelo de biofundición: una convergencia tecnológica
Multiómica, CRISPR y el auge de la “biocodificación”
En los últimos años, la comprensión de la biología y la genética ha experimentado un progreso extraordinario. Los aspectos clave se basan en algunas tecnologías novedosas.
La primera es la secuenciación y la genómica, que se han vuelto lo suficientemente económicas como para realizarse de forma rutinaria por menos de 1,000 dólares por organismo.
Ahora se combina con muchas otras “-ómicas” (transcriptómica, proteómica, metabolómica, epigenómica, microbiómica, biología espacial) para crear multiómicauna comprensión holística de todos los múltiples niveles de complejidad en los organismos vivos.
Otra tecnología novedosa es XNUMX parece ser, una nueva forma de edición genética descubierta en 2012, que desde entonces se ha convertido en la forma más potente de editar los genes de todo tipo de organismos, incluso para curar enfermedades raras.
Por último, la aparición del big data, la IA y otras formas de análisis avanzado proporcionó a los biólogos las herramientas para procesar y comprender la avalancha de datos que ha generado la multiómica.
Al combinarse, surge una capacidad completamente nueva.
La combinación de toneladas de datos de multiómica biológica real con análisis de IA significa que todo el proceso para crear moléculas complejas puede ser mapeado, modelado e incluso simulado por completo. in silicoEsto abre la posibilidad de probar prácticamente miles de posibilidades o crear desde cero proteínas completamente nuevas con propiedades novedosas.
Gracias a CRISPR, introducir estas ideas en microorganismos o plantas reales nunca ha sido tan rápido, preciso y sencillo, transformándolos en fábricas biológicas bien controladas, o "biofundiciones", una subsección de la biología sintética.
Dado que el ADN es esencialmente un código biológico, la facilidad para crear organismos genéticamente modificados (OGM) y diseñar nuevos biosistemas hace que la biología se asemeje mucho a la programación informática.
“Piensen en una célula. Es como una pequeña máquina que funciona con código digital, muy similar a una computadora, solo que en este caso el código, en lugar de ceros y unos, son A, T, C y G. Así que la biología sintética consiste en programar células como programamos computadoras, modificando el código de ADN que contienen. Somos como programadores celulares a sueldo. Nuestro trabajo es lograr que la célula haga lo que nuestros clientes desean.”
Jason Kelly, director ejecutivo de Ginkgo Bioworks
Del plástico al perfume: lo que las biofundiciones pueden construir.
Muchos de los productos químicos que actualmente produce la industria química podrían, en teoría, sustituirse por medios biológicos. Ya sea con la misma molécula producida por organismos vivos o con sustitutos de propiedades similares.
Por ejemplo, los microorganismos del suelo y las plantas producen habitualmente pequeñas cantidades de fertilizante, etanol o etileno, moléculas que actualmente se producen en masa por la industria química. Por lo tanto, una mayor producción o un menor coste de producción por parte de un organismo vivo podría tener un impacto de carbono mucho menor.
Otro objetivo es reducir la dependencia de los combustibles fósiles mediante la producción de polímeros, incluidos textiles y plásticos (1,4-butanodiol, 1,3-propanodiol, polihidroxialcanoatos, poliláctico, etc.), a través de rutas metabólicas biológicas.
En teoría, fragancias de alto valor, aminoácidos, vitaminas, seda, sabores como la vainillina e ingredientes cosméticos como el escualano o el ácido hialurónico también podrían producirse en masa de forma natural y a bajo coste.
Y, por supuesto, muchas moléculas biológicas de reciente invención pueden formar vacunas sintéticas, tratamientos contra el cáncer, proteínas alternativas y fuentes de alimentos (carne cultivada, etc.).
Por último, de esta forma se pueden producir productos totalmente novedosos. Por ejemplo, el micelio de los hongos puede crear una alternativa viable al cuero y otros textiles. O bien, las emisiones de carbono pueden reciclarse directamente para convertirlas en productos útiles antes de que lleguen a la atmósfera.
El modelo de negocio de investigación como servicio
Construyendo sinergias
Si bien la tecnología para lograrlo ha madurado, en la práctica no resulta tan sencillo reescribir por completo el metabolismo de un ser vivo real, manteniendo al mismo tiempo su productividad.
Por ello, una tendencia creciente es la subcontratación de esta tarea a empresas especializadas que cuentan con el equipo, la experiencia y el material biológico adecuado para llevarla a cabo. Este modelo de «Investigación como servicio», también conocido como «organismos bajo demanda», permite que diferentes proyectos y conceptos se complementen entre sí en diversos ámbitos.
Por ejemplo, un microorganismo desarrollado previamente para la absorción de emisiones de carbono también puede utilizar ese carbono para producir etileno, un precursor clave en innumerables reacciones de síntesis química. Sin embargo, una empresa centrada en créditos de carbono no tendría experiencia ni uso inmediato del etileno, mientras que una empresa química podría no tener una fuente de carbono a mano. Pero al utilizar el mismo proveedor de biofundición, ambas empresas pueden desarrollar sinergias y hacer que el proceso sea más eficiente.
Del mismo modo, un nuevo método optimizado para modificaciones genéticas puede aplicarse a docenas de aplicaciones diferentes, amortizando así el coste de I+D en una gama más amplia de proyectos.
Ginkgo Bioworks: El “ADN” de la biología sintética
Ninguna empresa ha estado más a la vanguardia de los "organismos a demanda" que Ginkgo Bioworks. Desde su fundación en 2008 por cinco científicos del MIT, la empresa se dedicó a producir bacterias transgénicas para aplicaciones industriales, y la biotecnología, que suele ser el foco de dicha actividad, quedó relegada a un segundo plano.
Ginkgo fue la primera empresa de biotecnología en unirse al famoso programa acelerador de startups Y Combinator en 2014. La empresa salió a bolsa en 2021 mediante una fusión con una SPAC y logró obtener el símbolo bursátil DNA en la Bolsa de Nueva York, que anteriormente pertenecía a la pionera en biotecnología Genentech (antes de su adquisición por Roche).
Ginkgo Bioworks Holdings, Inc. (DNA -7.49%)
Desde entonces, Gingko Bioworks se ha convertido en un socio clave de muchas empresas industriales, farmacéuticas y agrícolas.

Fuente: Bioworks de Gingko
Por ejemplo, desarrolló nuevos organismos para diversos programas de investigación:
- Microorganismos programables para enfermedades intestinales.
- Biorremediación de microplásticos.
- Terapias y vacunas de ARN.
- Reciclaje de residuos y contaminantes.
- Control de enfermedades críticas de la soja en Brasil.
- Sustituir los fertilizantes nitrogenados por bacterias
- Cannabinoides.
- Fabricación optimizada de productos biológicos y péptidos
- Producción de principios activos farmacéuticos (API) mediante biocatálisis y fermentación a gran escala.
- Soluciones de diagnóstico molecular, mediante una base de datos de enzimas propia y diseñadores de enzimas expertos.
- Terapia celular y edición genética.
El giro estratégico de Gingko: Vender bioseguridad para laboratorios autónomos
Vender el negocio de la bioseguridad
Durante la pandemia de COVID-19, Gingko expandió rápidamente su negocio de bioseguridad, una actividad que monitorea los riesgos biológicos, principalmente para gobiernos. Posteriormente, evolucionó hasta convertirse en una plataforma de biorradar integral.
Esa actividad empresarial aportó beneficios invaluables durante la pandemia a través de nuestros programas de pruebas estatales y nacionales, y generó ingresos anuales máximos superiores a los 300 millones de dólares. Nos enorgullece haber contribuido a la reapertura de más de 5,000 escuelas en todo el país.
Sin embargo, esta actividad está relativamente desconectada del resto de los proyectos de Gingko Bioworks. Por ello, la dirección de la empresa ha decidido venderla a un consorcio de inversores, creando una nueva entidad privada independiente llamada Tower Biosecurity, y Gingko conservará una participación del 20%.
De proveedor de servicios a alianzas de alto valor
La actividad de “organismos a demanda” constituye actualmente el núcleo del negocio de la empresa, siendo los segmentos más importantes los de alimentación y agricultura, y farmacia y biotecnología. Sin embargo, sus ingresos disminuyeron entre el cuarto trimestre de 2024 y el cuarto trimestre de 2025, debido a la caída general de la inversión en biotecnología durante ese periodo.

Fuente: Bioworks de Gingko
Este segmento ha sufrido una relativa incertidumbre respecto a su modelo de negocio. Inicialmente, Gingko planeaba ofrecer únicamente la capacidad de investigación como un servicio puro, con un precio fijo y un objetivo claro. Esto hizo que Gingko fuera extremadamente popular como socio de investigación.
Sin embargo, esto también significaba que no había regalías residuales ni ingresos adicionales una vez finalizado el proyecto, lo que implicaba que Gingko estaba atrapado en un ciclo interminable de nuevos proyectos, donde su destreza tecnológica no se traducía realmente en ingresos.
Desde entonces, ha comenzado a desarrollar nuevos organismos con una estructura de asociación más definida. Por ejemplo, La consecución de un hito importante en un proyecto con Merck, que generó un pago de 9 millones de dólares en el cuarto trimestre de 2024. y pagos mayores más adelante, en la fase 2 del proyecto.
La empresa se tomó muy en serio la necesidad de reestructurarse para generar mayor flujo de caja, y por ello realizó un gran esfuerzo para reducir el consumo de efectivo, que disminuyó un 73 % el año pasado. Además, la empresa no tiene deudas significativas, lo que reduce aún más los riesgos financieros.

Fuente: Bioworks de Gingko
El auge del laboratorio de robots modulares y autónomos
Si bien la ingeniería celular fue el eje central de la empresa en el pasado, su futuro reside ahora en el uso de la IA y sus propios laboratorios automatizados para reducir costes y mejorar la creación de nuevas biofundiciones.
Laboratorios automatizados Se trata de una tecnología en la que Gingko lleva trabajando un tiempo, ya que todavía hoy la mayor parte del trabajo en los laboratorios biológicos consiste en tareas manuales repetitivas y tediosas, que a menudo consumen la mayor parte del tiempo de una plantilla con másteres y doctorados.
Para cambiar este método, ha creado una plataforma modular automatizada, capaz de realizar sin intervención humana tareas de laboratorio como el cultivo de células, la transferencia de productos químicos, el análisis microscópico, etc.

Fuente: Bioworks de Gingko
La característica más importante de este diseño es su modularidad. Cada módulo puede conectarse con otro para crear una especie de “cadena de ensamblaje” para experimentos científicos y bioanálisis.
Esta solución se combina con una oferta de software, creando una solución flexible que se puede adaptar y modificar en tan solo días u horas, en comparación con infraestructuras de investigación más rígidas que requieren meses de costosa reconfiguración para nuevos proyectos.

Fuente: Bioworks de Gingko
Esta combinación proporciona tanto la flexibilidad necesaria para la investigación (en comparación con la producción en masa) como la automatización necesaria para acelerar la investigación y reducir los costes, ya que el laboratorio automatizado puede trabajar más rápido que un ser humano y las 24 horas del día, los 7 días de la semana.
Gingko planea ofrecer esta tecnología en dos formatos:
- “Construye tu propio laboratorio”, donde la empresa fabrica y da servicio a los módulos de laboratorio automatizados, pero las operaciones diarias y la propiedad pertenecen al cliente.
- Acceda al laboratorio autónomo de vanguardia de Ginkgo mediante la contratación directa del servicio.
Datapoint: Generando 10,000 experimentos en semanas
Si bien la solución de automatización genera los datos biológicos, Datapoint los procesa para convertirlos en información útil.
El elemento clave es la rápida generación de datos que puedan orientar futuras hipótesis y la rápida iteración de nuevos experimentos para seguir avanzando.
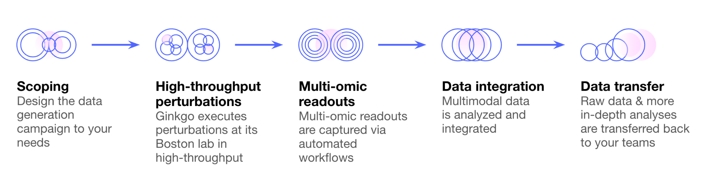
Fuente: Ginkgo Bioworks
Con este servicio, Ginkgo puede proporcionar datos que pertenecen íntegramente al cliente, lo que supone una ventaja competitiva en las colaboraciones con otras empresas biotecnológicas o farmacéuticas.
Es posible generar datos en tan solo 3 semanas, con más de 10,000 perturbaciones químicas y genéticas in vitro en cada tipo de célula, y una amplia gama de métodos analíticos disponibles para estudiar los resultados.
El mismo sistema puede utilizarse para la generación rápida de nuevos anticuerpos, un tipo de molécula que se está convirtiendo rápidamente en un medicamento clave en oncología y otras áreas médicas. Ginkgo puede analizar hasta 2,400 anticuerpos diferentes en paralelo, gracias a una infraestructura de laboratorio automatizado valorada en 1 millones de dólares.
Investigación biológica impulsada por IA
Gingko estableció una alianza con OpenAI para utilizar ChatGPT 5 en el contexto de la investigación biológica. Se observó una mejora drástica en la productividad.
“La empresa informa que el sistema redujo los costos de las reacciones de síntesis de proteínas sin células en un 40 % en comparación con la tecnología más avanzada, al tiempo que ejecutó 36 000 condiciones experimentales a lo largo de seis ciclos iterativos.”
La participación humana se limitó principalmente a la preparación de reactivos, la carga y descarga, y la supervisión del sistema, mientras que el diseño experimental, la ejecución, la interpretación de datos y la generación de hipótesis fueron gestionados por el laboratorio autónomo controlado por GPT-5.
El modelo utilizado se ha publicado como código abierto y La comunidad científica puede solicitar la mezcla de reacción sin células mejorada con IA., convirtiendo a Gingko en una importante herramienta de investigación de código abierto para científicos de todo el mundo.
Gingko también era Recibió 47 millones de dólares del gobierno estadounidense. para desarrollar un gran centro de investigación para el Misión Génesis, un sitio de 32,000 pies cuadrados conocido como el Capacidad de fenotipado molecular microbiano (M2PC)Albergará más de 100 instrumentos analíticos automatizados y se espera que esté plenamente operativo para investigadores de todo el mundo en 2030.
“El equipo aprovechará la IA avanzada para descifrar la función de las proteínas y las vías metabólicas, automatizar la generación y recopilación de datos, e integrar los sistemas experimentales y de supercomputación del Departamento de Energía con empresas de biotecnología e IA.”
Perspectivas a largo plazo: ¿El ginkgo finalmente es rentable?
Gingko, creador del modelo de negocio de biofundición y actor importante en bioseguridad, se está reinventando como líder en la automatización de la investigación biológica y socio clave en tecnología de I+D basada en inteligencia artificial.
A medida que la biología se fusiona con la IA, muchos procesos industriales serán reemplazados progresivamente por alternativas biotecnológicas más sostenibles, neutras en carbono, no tóxicas y más económicas. En esta visión del futuro, las formas de vida son tan programables como el código informático, pero con un impacto aún mayor en el mundo real.
Esto representa una gran oportunidad para Gingko Bioworks, ya sea para el proyecto en el que ya está trabajando o para que su diseño de laboratorio automatizado se convierta en un estándar para la mayoría de los equipos de investigación a largo plazo.
Si a esto se le suma una mejora en su modelo de negocio de ingeniería celular (con mayores regalías y contratos de reparto de ingresos más justos), debería contribuir a que Gingko sea rentable en los próximos años.
(También puede leer más sobre otras empresas de biología sintética en “Las 5 principales empresas públicas de biología sintética")











