Biotecnologia
Próxima Geração de CRISPR Melhora a Precisão na Terapia Genética

Tornando a Edição de Genes Mais Precisa
Até recentemente, as modificações genéticas eram bastante grosseiras, inserindo uma nova sequência genética aleatoriamente nos organismos alvo.
O método de inserção também era muito destrutivo. Como resultado, apenas bactérias e plantas eram rotineiramente modificadas geneticamente, e qualquer edição de genes em organismos como mamíferos (incluindo humanos) era complexa, cara e lenta.
Isso mudou parcialmente com a tecnologia CRISPR, que abriu caminho para a edição de genes precisa e controlada, resultando na aprovação da primeira terapia genética para doenças genéticas humanas no final de 2023.
No entanto, a CRISPR ainda não é perfeita, às vezes resultando em modificações genéticas indesejadas.
Isso pode ter mudado com uma descoberta revolucionária de três pesquisadores do MIT.
Eles anunciaram um novo método que permite uma confiabilidade radicalmente melhorada na edição de genes, abrindo caminho para a criação de novas terapias.
Eles publicaram seus resultados na prestigiosa revista científica Nature1, sob o título “Engineered prime editors with minimal genomic errors”.
Da CRISPR Padrão para Edição de Primeira Linha
Desde a aprovação das primeiras terapias baseadas em CRISPR-Cas9, a ideia de editar confiavelmente os genomas de pacientes para curá-los não é mais ficção científica. No entanto, a tecnologia CRISPR não sempre modifica o gene alvo da maneira como os cientistas pretendem.
A sistema CRISPR consiste em uma enzima chamada Cas9 que pode cortar o DNA de fita dupla em um local específico, juntamente com um RNA guia que diz a Cas9 onde cortar.
Os pesquisadores adaptaram essa abordagem para cortar sequências de genes defeituosas ou inserir novas, seguindo um modelo de RNA.
Desde 2019, os pesquisadores do MIT publicaram um novo conceito chamado edição de primeira linha, que é mais preciso do que a edição de genes regular CRISPR-Cas9. Como resultado, tem menos efeitos fora do alvo e menos chance de causar problemas de saúde extras a pacientes já fracos.
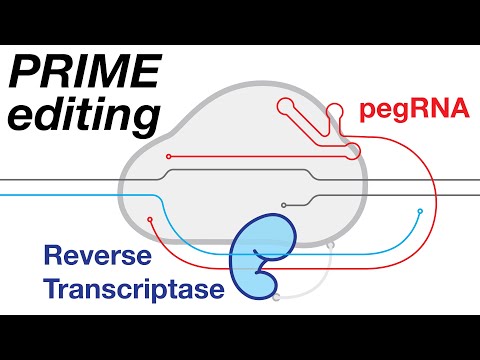
A edição de primeira linha usa uma Cas9 modificada fundida com uma enzima transcriptase reversa, permitindo que ela realize todas as modificações de base genética possíveis, bem como pequenas inserções e deleções de sequências genéticas.
Portanto, a longo prazo, a edição de primeira linha é esperada para se tornar a versão atualizada e mais confiável da edição de genes baseada em CRISPR.

Fonte: Benjamin McLeod
Por exemplo, editores de primeira linha foram usados com sucesso em 2025 para tratar um paciente com doença granulomatosa crônica (DGC), uma doença genética rara que afeta glóbulos brancos.
“Em princípio, essa tecnologia poderia ser usada eventualmente para abordar muitas centenas de doenças genéticas, corrigindo mutações pequenas diretamente em células e tecidos.”
Vikash Chauhan – Instituto Koch de Pesquisa de Câncer do MIT
Mas precisava de um pouco de melhoria antes de estar pronto para uso em células e corpos humanos.
Como a Edição de Primeira Linha Melhora a Precisão de Inserção de DNA
A edição de primeira linha corta apenas uma das fitas complementares da sequência de DNA alvo, abrindo uma aba onde uma nova sequência pode ser inserida.
Uma vez que a nova sequência tenha sido copiada, no entanto, ela deve competir com a fita de DNA antiga para ser incorporada ao genoma.
Se a fita antiga vencer a nova, a aba extra de DNA recém-criada pode ser incorporada acidentalmente em outro lugar, dando origem a erros.
Tais erros poderiam causar câncer ao se inserir aleatoriamente no genoma, um risco claro que precisa ser reduzido.
Com a versão mais recente dos editores de primeira linha, a taxa de erro varia de um erro por sete edições para um erro por 121 edições para diferentes modos de edição, o que ainda é alto demais.
“As tecnologias que temos agora são realmente muito melhores do que as ferramentas de terapia genética anteriores, mas sempre há uma chance de consequências não intencionais,”
Vikash Chauhan – Instituto Koch de Pesquisa de Câncer do MIT
Grande Salto na Confiabilidade da Edição de Primeira Linha
Em 2023, os pesquisadores do MIT descobriram que algumas versões mutadas da proteína Cas9 usada na edição de primeira linha às vezes faziam o corte um ou dois bases mais longe na sequência de DNA, em vez de sempre no mesmo local.
Isso tornou as fitas de DNA antigas menos estáveis, então elas se degradam, tornando mais fácil para as novas fitas serem incorporadas sem introduzir erros.
Neste novo estudo de 2025, os pesquisadores identificaram múltiplas mutações de Cas9 que reduziram a taxa de erro para 1/20 do valor original.
Quando combinaram essas mutações artificialmente em uma única proteína Cas9, reduziram a taxa de erro para 1/36 do valor original.
“Este artigo descreve uma nova abordagem para edição de genes que não complica o sistema de entrega e não adiciona etapas adicionais, mas resulta em uma edição muito mais precisa com menos mutações indesejadas,”
Não satisfeitos com isso, eles também usaram um sistema de edição de primeira linha que tem uma proteína de ligação a RNA que estabiliza as extremidades do modelo de RNA de forma mais eficiente.
Chamado de vPE, a versão final de sua ferramenta de edição de genes tinha uma taxa de erro apenas 1/60 do original, ou apenas 101-543 edições, dependendo dos modos de edição usados.
Deslize para rolar →
| Versão do Editor de Primeira Linha | Taxa de Erro Aproximada | Melhoria vs Original |
|---|---|---|
| Editor de Primeira Linha Original | 1 erro por 7–121 edições | Referência |
| Variantes Mutadas de Cas9 | 1/20–1/36 da taxa de erro original | Até 36 vezes mais preciso |
| vPE (estabilizado por RNA) | 1/60 da taxa de erro original | Até 60 vezes mais preciso |
Próximos Passos
Outro obstáculo da edição de genes sempre foi a entrega das proteínas de edição de genes e DNA/RNA dentro do núcleo das células alvo, ou direcionar apenas tecidos específicos no corpo.
Portanto, isso será o próximo foco dos pesquisadores, especialmente porque as técnicas de edição de primeira linha são limitadas por uma entrega pobre em comparação com os sistemas “tradicionais” de CRISPR-Cas9 menores e mais simples.
Eles também acreditam que essa ferramenta tem o potencial de acelerar o progresso na biotecnologia como um todo, não apenas para terapias de edição de genes.
Primeiro, a técnica e a descoberta de que a modificação da proteína Cas9 pode melhorar sua confiabilidade podem ser implantadas em todas as tecnologias de edição de genes baseadas em CRISPR, não apenas na edição de primeira linha.
Segundo, isso pode se tornar um impulso poderoso para outros projetos de pesquisa que usam edição de genes e genoma como ferramenta de pesquisa. Por exemplo, encontrar respostas sobre como os tecidos se desenvolvem, como as populações de células cancerígenas evoluem e como as células respondem ao tratamento com drogas.
“Editores de genoma são usados extensivamente em laboratórios de pesquisa.
A parte terapêutica é emocionante, mas estamos realmente animados para ver como as pessoas começam a integrar nossos editores em seus fluxos de trabalho de pesquisa.”
Vikash Chauhan – Instituto Koch de Pesquisa de Câncer do MIT
Por fim, as mutações encontradas para melhorar a confiabilidade de Cas9 podem não ter sido todas encontradas neste estudo. Portanto, uma análise e otimização adicionais desse novo conceito podem produzir resultados ainda melhores no futuro.
Investindo em Edição de Genes
Illumina
(ILMN )
Enquanto as outras -ômicas (proteômica, transcriptômica, etc.) são importantes, quase todas articulam de uma forma ou de outra em torno da genômica, o manual de instruções central de cada célula viva.
E, de longe, o maior produtor de máquinas de sequenciamento de genoma é a Illumina. A empresa está focada na leitura de sequências genéticas curtas, que é a usada para detecção de câncer. Atualmente, tem 22.000+ sequenciadores instalados em 165 países.
Cerca de metade dos consumíveis das máquinas de sequenciamento da Illumina são usados em aplicações clínicas, com a outra metade usada em laboratórios de pesquisa públicos e privados. Em aplicações clínicas, metade da demanda vem da oncologia.

Fonte: Illumina
À medida que a genômica e a multiômica se tornam o centro do processo de descoberta de drogas, bem como diagnósticos de câncer, os equipamentos da Illumina devem estar em alta demanda.
A empresa espera que a demanda por NGS (Sequenciamento de Nova Geração) cresça 18% CAGR para aplicações clínicas e 6% CAGR para pesquisa, impulsionando o mercado total endereçável (TAM) do setor de $100B para clínicas e $25B para pesquisa até 2033.

Fonte: Illumina
A Illumina teve uma história complicada com a empresa de biópsia líquida Grail (GRAL -0.36%), que foi uma spin-off da Illumina, posteriormente readquirida e agora forçada a se separar novamente por autoridades de concorrência nos EUA e UE.
Com esse problema resolvido, a Illumina pode retomar seu crescimento de longo prazo e aumento do preço das ações, especialmente porque, em última análise, os testes de biópsia líquida da Grail provavelmente ainda dependerão dos sequenciadores da Illumina.
Enquanto isso, mais terapias genéticas também aumentarão o uso dos sequenciadores da Illumina em ambientes de pesquisa e clínicos.
(Você também pode ler uma análise mais detalhada do negócio da Illumina, tecnologias futuras e história no relatório de investimento dedicado.)
Últimas Notícias e Desenvolvimentos da Illumina (ILMN)
Estudo Referenciado
1. Chauhan, V.P., Sharp, P.A. & Langer, R. Engineered prime editors with minimal genomic errors. Nature (2025). https://doi.org/10.1038/s41586-025-09537-3