BioTech
Die Biofoundry-Revolution: Leben als Fabrik programmieren

Der Wandel von chemischen zu biologischen Fabriken
Wie digitaler Code synthetische Chemikalien ersetzt
Sobald die ersten Wissenschaftler erkannten, dass die materielle Welt um sie herum aus getrennten, reinen Bestandteilen besteht, begannen sie, diese besser zu verstehen. Die frühen alchemistischen Bemühungen ebneten den Weg für die Wissenschaftler der Aufklärung und der frühen Neuzeit, die die einzelnen Elemente und die Grundlagen der Biologie – Zellen, DNA usw. – entdeckten.
Zur gleichen Zeit schuf die chemische Industrie die Anfänge der pharmazeutischen Industrie, indem sie synthetische chemische Arzneimittel einsetzte, um biologische Prozesse bei Patienten zu verändern, beispielsweise durch die Verwendung von Salicylsäure (Aspirin) zur Fiebersenkung.
Die in Medizin und Industrie verwendeten Chemikalien wurden zunehmend komplexer. Generell gilt jedoch: Je komplexer ein Molekül ist, desto schwieriger lässt es sich mit künstlichen chemischen Methoden synthetisieren. Bei den komplexesten Proteinen oder biochemischen Verbindungen ist dies sogar schlichtweg unmöglich.
Dann ermöglichte die Bioingenieurtechnik die Produktion von billigem und sicherem Insulin, Wachstumshormonen, Antikörpern usw. mithilfe von GVO-Mikroben, wodurch das Gebiet der Biotechnologie als ein verwandtes, aber eigenständiges Gebiet neben der Pharmazie entstand.
Dies war eine gewaltige Revolution in der Biochemie und Medizin, die plötzlich in großen Mengen und zu geringen Kosten Verbindungen herstellte, die zuvor extrem teuer oder unmöglich zu beschaffen waren.
Heute konvergieren viele neue Technologien (Big Data, KI, Automatisierung, präzise Gentechnik, fortgeschrittene Analytik usw.) und eröffnen eine neue Ära der Biowissenschaften: die Biofoundry-Revolution.
Jenseits der Natur: Organismen für die Industrie neu gestalten
Das Biotechnologiezeitalter war geprägt vom Einsatz künstlicher genetischer Veränderungen, um Mikroorganismen zur Produktion von gewünschten Biomolekülen, meist medizinischen Produkten, zu bewegen. Dies erwies sich als außerordentlich profitabel, da viele dieser Moleküle lebensrettende oder hochwertige Produkte sind, die zuvor nur in geringen Mengen und mit aufwändigen Methoden gewonnen werden konnten.
Dies birgt jedoch die systembedingte Einschränkung, dass nur das nachgebildet werden kann, was bereits in lebenden Organismen existiert. Bis heute ist die Produktion vieler Materialien und nützlicher Moleküle jedoch von künstlich hergestellten Chemikalien abhängig, die mithilfe toxischer oder CO₂-emittierender Verfahren gewonnen werden.
Während die Umstellung unseres Energiesystems auf Elektrofahrzeuge, Batterien und erneuerbare Energien wichtig ist, ist die Suche nach umweltfreundlicheren Alternativen zur chemischen Produktion ebenso wichtig für die Lösung der meisten Probleme der modernen Welt: Plastikverschmutzung, Klimawandel, nachhaltige Landwirtschaft, emissionsfreie Industrieproduktion, Biosicherheit, unheilbare Krankheiten, regenerative Medizin, Langlebigkeitsbehandlungen usw.
Und für all diese Probleme wird nun eine Lösung eingesetzt: das Biofoundry-Modell.
Wie das Biofoundry-Modell funktioniert: Eine technologische Konvergenz
Multiomics, CRISPR und der Aufstieg des „Bio-Codierens“
In den letzten Jahren hat das Verständnis von Biologie und Genetik enorme Fortschritte gemacht. Die wichtigsten Erkenntnisse basieren auf einigen wenigen neuen Technologien.
Die erste ist die Sequenzierung und Genomik, die mittlerweile so günstig geworden ist, dass sie routinemäßig für weniger als 1,000 US-Dollar pro Organismus durchgeführt werden kann.
Sie wird nun mit vielen anderen „-omics“-Technologien (Transkriptomik, Proteomik, Metabolomik, Epigenomik, Mikrobiomik, räumliche Biologie) kombiniert, um … zu schaffen. Multiomik, ein ganzheitliches Verständnis aller vielfältigen Komplexitätsebenen in lebenden Organismen.
Eine weitere neuartige Technologie ist CRISPR, eine neue Methode der Genbearbeitung, die 2012 entdeckt wurde und sich seither zur leistungsstärksten Methode zur Bearbeitung der Gene aller Arten von Organismen entwickelt hat, einschließlich zur Heilung seltener Krankheiten.
Schließlich gaben das Aufkommen von Big Data, KI und anderen Formen fortgeschrittener Analytik den Biologen die Werkzeuge an die Hand, um die durch die Multiomics entstandene Datenflut zu verarbeiten und zu interpretieren.
Wenn beides zusammenkommt, entsteht eine völlig neue Fähigkeit.
Die Kombination von Unmengen an Daten aus realen biologischen Multiomics-Studien mit KI-Analysen ermöglicht es, den gesamten Prozess der Herstellung komplexer Moleküle abzubilden, zu modellieren und sogar vollständig zu simulieren. in silicoDies eröffnet die Möglichkeit, praktisch tausende von Möglichkeiten zu testen oder völlig neue Proteine mit neuartigen Eigenschaften von Grund auf zu entwickeln.
Dank CRISPR war es noch nie so schnell, präzise und einfach, diese Ideen in echte Mikroorganismen oder Pflanzen einzubringen und sie in gut kontrollierte biologische Fabriken oder „Biofoundries“ zu verwandeln, einem Teilgebiet der synthetischen Biologie.
Da die DNA im Wesentlichen ein biologischer Code ist, rückt die Leichtigkeit, mit der sich GVOs herstellen und neue Biosysteme entwerfen lassen, die Biologie der Computerprogrammierung sehr nahe.
„Stellen Sie sich eine Zelle vor. Sie ist wie eine kleine Maschine, die mit digitalem Code arbeitet, ähnlich einem Computer. Nur dass der Code in diesem Fall – statt Nullen und Einsen – aus A, T, C und G besteht. Synthetische Biologie programmiert Zellen also wie Computer, indem sie den DNA-Code in ihnen verändert. Wir sind sozusagen Zellprogrammierer, die man beauftragen kann. Unsere Aufgabe ist es, die Zelle so zu steuern, wie es unsere Kunden wünschen.“
Jason Kelly – CEO von Ginkgo Bioworks
Von Plastik zu Parfüm: Was Biofoundries herstellen können
Viele der derzeit in der chemischen Industrie hergestellten Chemikalien könnten theoretisch durch biologisch hergestellte Alternativen ersetzt werden. Entweder durch dasselbe Molekül, das von lebenden Organismen produziert wird, oder durch Ersatzstoffe mit ähnlichen Eigenschaften.
Beispielsweise produzieren Bodenmikroorganismen und Pflanzen routinemäßig in geringen Mengen Dünger, Ethanol oder Ethylen – alles Moleküle, die derzeit von der chemischen Industrie in großen Mengen hergestellt werden. Eine höhere Ausbeute oder eine kostengünstigere Produktion durch einen lebenden Organismus könnte also eine deutlich geringere CO₂-Bilanz zur Folge haben.
Ein weiteres Ziel ist die Verringerung der Abhängigkeit von fossilen Brennstoffen durch die Herstellung von Polymeren, einschließlich Textilien und Kunststoffen (1,4-Butandiol, 1,3-Propandiol, Polyhydroxyalkanoate, Polymilchsäure usw.), über biologische Stoffwechselwege.
Hochwertige Duftstoffe, Aminosäuren, Vitamine, Seide, Aromen wie Vanillin und kosmetische Inhaltsstoffe wie Squalan oder Hyaluronsäure könnten zumindest theoretisch auch auf natürliche Weise in großen Mengen und zu geringen Kosten hergestellt werden.
Und natürlich können viele neu erfundene biologische Moleküle zur Herstellung synthetischer Impfstoffe, Krebsmedikamente, alternativer Protein- und Nahrungsquellen (z. B. kultiviertes Fleisch) verwendet werden.
Schließlich lassen sich auf diese Weise völlig neuartige Produkte herstellen. So kann beispielsweise Pilzmyzel eine praktikable Alternative zu Leder und anderen Textilien bilden. Oder Kohlenstoffemissionen können direkt zu nützlichen Produkten recycelt werden, bevor sie überhaupt in die Atmosphäre gelangen.
Das Geschäftsmodell „Forschung als Dienstleistung“
Synergien aufbauen
Auch wenn die Technologie hierfür ausgereift ist, ist es in der Praxis nicht so einfach, den Stoffwechsel eines realen Lebewesens vollständig umzuschreiben und es gleichzeitig produktiv zu halten.
Aus diesem Grund geht der Trend zunehmend dahin, diese Aufgabe an spezialisierte Unternehmen auszulagern, die über die nötige Ausrüstung, Expertise und das geeignete biologische Material verfügen. Dieses „Forschungs-als-Dienstleistung“-Modell, auch „Organismen-auf-Abruf“ genannt, ermöglicht es, dass verschiedene Projekte und Konzepte bereichsübergreifend zusammenarbeiten.
Ein Mikroorganismus, der ursprünglich zur Absorption von Kohlenstoffemissionen entwickelt wurde, kann diesen Kohlenstoff beispielsweise auch zur Herstellung von Ethylen nutzen, einem wichtigen Vorprodukt für unzählige chemische Synthesereaktionen. Ein auf CO₂-Zertifikate spezialisiertes Unternehmen hätte jedoch weder unmittelbare Verwendungsmöglichkeiten noch Erfahrung mit Ethylen, während ein Chemieunternehmen möglicherweise keine geeignete Kohlenstoffquelle zur Verfügung hat. Durch die Zusammenarbeit mit demselben Biofoundry-Auftragnehmer können beide Unternehmen jedoch Synergien nutzen und den Prozess effizienter gestalten.
In ähnlicher Weise kann eine neue, optimierte Methode für genetische Modifikationen für Dutzende verschiedener Anwendungen eingesetzt werden, wodurch sich die Kosten für Forschung und Entwicklung auf eine breitere Palette von Projekten verteilen.
Ginkgo Bioworks: Die „DNA“ der Synthetischen Biologie
Kein Unternehmen war im Bereich der „Organismen auf Abruf“ so führend wie Ginkgo Bioworks. Seit seiner Gründung im Jahr 2008 durch fünf MIT-Wissenschaftler widmete sich das Unternehmen der Produktion von GVO-Bakterien für industrielle Anwendungen, wobei die Biotechnologie, die üblicherweise im Mittelpunkt solcher Aktivitäten steht, nur eine untergeordnete Rolle spielte.
Ginkgo war 2014 das erste Biotechnologieunternehmen, das dem renommierten Start-up-Accelerator-Programm Y Combinator beitrat. Das Unternehmen ging 2021 durch eine SPAC-Fusion an die Börse und sicherte sich das NYSE-Tickersymbol DNA, das zuvor vom Biotech-Pionier Genentech (vor dessen Übernahme durch Roche) gehalten wurde.
Ginkgo Bioworks Holdings, Inc. (DNA -7.49 %)
Seitdem hat sich Gingko Bioworks zu einem wichtigen Partner zahlreicher Industrie-, Pharma- und Agrarunternehmen entwickelt.

Quelle: Gingko Bioworks
Zum Beispiel entwickelte es neue Organismen für verschiedene Forschungsprogramme:
- Programmierbare Mikroben zur Behandlung von Darmerkrankungen.
- Bioremediation von Mikroplastik.
- RNA-Therapeutika und -Impfstoffe.
- Recycling von Abfällen und Schadstoffen.
- Bekämpfung kritischer Sojabohnenkrankheiten in Brasilien.
- Stickstoffdünger durch Bakterien ersetzen
- Cannabinoide.
- Optimierte Herstellung von Biologika und Peptiden
- Herstellung von pharmazeutischen Wirkstoffen (API) durch Biokatalyse und Fermentation im größeren Maßstab.
- Molekulardiagnostische Lösungen durch eine firmeneigene Enzymdatenbank und erfahrene Enzymdesigner.
- Zelltherapie und Genomeditierung.
Gingkos Strategiewechsel: Biosicherheit für autonome Labore verkaufen
Verkauf des Biosecurity-Geschäfts
Während der COVID-Pandemie baute Gingko sein Geschäft mit Biosicherheit, einer Tätigkeit, die biologische Risiken hauptsächlich für Regierungen überwacht, rasch aus. Daraus entwickelte sich eine umfassende Bioradar-Plattform.
Dieses Geschäft leistete während der Pandemie durch unsere staatlichen und nationalen Testprogramme einen unschätzbaren Beitrag und erzielte einen jährlichen Spitzenumsatz von über 300 Millionen Dollar. Wir waren stolz darauf, zur Wiedereröffnung von über 5,000 Schulen landesweit beigetragen zu haben.
Diese Aktivität ist jedoch relativ unabhängig von den übrigen Projekten von Gingko Bioworks. Daher hat die Unternehmensleitung beschlossen, sie an ein Investorenkonsortium zu veräußern und ein neues, eigenständiges Privatunternehmen namens Tower Biosecurity zu gründen. Gingko behält dabei eine Beteiligung von 20 %.
Vom Dienstleister zu hochwertigen Partnerschaften
Die Bereitstellung von Organismen auf Abruf bildet derzeit das Kerngeschäft des Unternehmens, wobei die Bereiche Lebensmittel & Landwirtschaft sowie Pharma & Biotechnologie die größten Segmente darstellen. Allerdings sind die Umsätze in diesem Bereich zwischen dem vierten Quartal 2024 und dem vierten Quartal 2025 aufgrund eines allgemeinen Investitionsrückgangs im Biotechnologiesektor in diesem Zeitraum gesunken.

Quelle: Gingko Bioworks
Dieses Segment litt unter einer gewissen Unsicherheit hinsichtlich seines Geschäftsmodells. Ursprünglich plante Gingko, Forschungskapazitäten als reine Dienstleistung mit Festpreis und klar definiertem Endpunkt anzubieten. Dies machte Gingko als Forschungspartner äußerst beliebt.
Dies bedeutete jedoch auch, dass nach Abschluss des Projekts keine weiteren Lizenzgebühren oder zusätzliche Einnahmen anfielen, wodurch Gingko in einem endlosen Kreislauf neuer Projekte gefangen war, wobei sich die technologische Kompetenz nicht wirklich in Einnahmen umsetzen ließ.
Seitdem hat es begonnen, neue Organismen verstärkt in Partnerschaftsstrukturen zu entwickeln. Zum Beispiel die Erreichung eines wichtigen Meilensteins in einem Projekt mit Merck, was zu einer Auszahlung von 9 Millionen US-Dollar im vierten Quartal 2024 führt. und höhere Zahlungen später in Phase 2 des Projekts.
Die Notwendigkeit einer Restrukturierung zur Verbesserung des Cashflows wurde vom Unternehmen ernst genommen, und es wurden erhebliche Anstrengungen unternommen, den Cash-Burn zu reduzieren, der im vergangenen Jahr um 73 % gesunken ist. Gleichzeitig weist das Unternehmen keine nennenswerten Schulden auf, wodurch weitere finanzielle Risiken minimiert werden.

Quelle: Gingko Bioworks
Der Aufstieg des modularen, autonomen Roboterlabors
Wenn die Zelltechnik in der Vergangenheit das Herzstück des Unternehmens war, liegt seine Zukunft nun darin, mithilfe von KI und eigenen automatisierten Laboren die Kosten zu senken und die Entwicklung neuer Biofoundries zu verbessern.
Automatisierte Labore sind eine Technologie, an der Gingko schon seit einiger Zeit arbeitet, da auch heute noch der größte Teil der Arbeit in Biolaboren aus sich wiederholenden und mühsamen manuellen Aufgaben besteht, die oft den Großteil der Arbeitszeit von Mitarbeitern mit Master- und Doktortiteln in Anspruch nehmen.
Um diese Methode zu ändern, wurde eine automatisierte modulare Plattform entwickelt, die in der Lage ist, Laboraufgaben wie die Kultivierung von Zellen, den Transfer von Chemikalien, mikroskopische Analysen usw. ohne menschliches Eingreifen durchzuführen.

Quelle: Gingko Bioworks
Das wichtigste Merkmal dieses Designs ist seine Modularität. Jedes Element kann mit einem anderen verbunden werden, um eine Art „Montagekette“ für wissenschaftliche Experimente und Bioanalysen zu schaffen.
Diese Lösung wird mit einem Softwareangebot kombiniert, wodurch eine flexible Lösung entsteht, die im Vergleich zu starreren Forschungsinfrastrukturen, die für neue Projekte monatelange, kostspielige Neukonfigurationen erfordern, in nur wenigen Tagen oder Stunden angepasst und geändert werden kann.

Quelle: Gingko Bioworks
Diese Kombination bietet sowohl die für die Forschung notwendige Flexibilität (im Vergleich zur Massenproduktion) als auch die Automatisierung, die erforderlich ist, um die Forschung zu beschleunigen und die Kosten zu senken, da das automatisierte Labor schneller arbeiten kann als ein Mensch und rund um die Uhr verfügbar ist.
Gingko plant, diese Technologie in zwei Formaten anzubieten:
- „Bauen Sie Ihr eigenes Labor“, wobei das Unternehmen die automatisierten Labormodule herstellt und wartet, die tägliche Betriebsführung und das Eigentum jedoch beim Kunden liegen.
- Zugang zu Ginkgos eigenem autonomen Spitzenlabor erhalten Sie durch direkte Beauftragung des Dienstleisters.
Datenpunkt: Generierung von 10,000 Experimenten innerhalb weniger Wochen
Während die Automatisierungslösung die biologischen Daten generiert, verarbeitet Datapoint diese zu nützlichen Erkenntnissen.
Das Schlüsselelement ist die schnelle Generierung von Daten, die als Grundlage für weitere Hypothesen dienen können, und die schnelle Wiederholung neuer Experimente, um weiter voranzukommen.
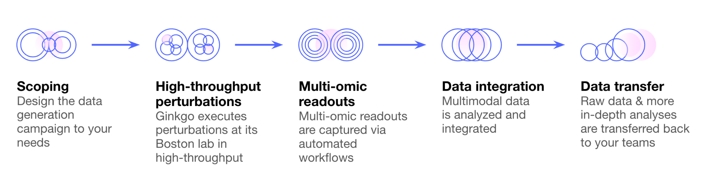
Quelle: Ginkgo Bioworks
Mit diesem Service kann Ginkgo Daten bereitstellen, die vollständig dem Kunden gehören, was einen Wettbewerbsvorteil bei Partnerschaften mit anderen Biotech- oder Pharmaunternehmen darstellt.
Die Datenerhebung kann in nur 3 Wochen erfolgen, wobei über 10,000 chemische und genetische In-vitro-Veränderungen in jedem Zelltyp möglich sind und eine breite Auswahl an Analysemethoden zur Untersuchung der Ergebnisse zur Verfügung steht.
Dasselbe System kann zur schnellen Erzeugung neuer Antikörper eingesetzt werden, einem Molekültyp, der sich in der Onkologie und anderen medizinischen Bereichen schnell zu einem Schlüsselmedikament entwickelt. Dank einer automatisierten Nasslabor-Infrastruktur im Wert von einer Milliarde Dollar kann Ginkgo bis zu 2,400 verschiedene Antikörper parallel testen.
KI-gestützte Bioforschung
Gingko ging eine Partnerschaft mit OpenAI ein, um ChatGPT 5 im Bereich der Bioforschung einzusetzen. Das Unternehmen berichtete von einer drastischen Produktivitätssteigerung.
„Das Unternehmen berichtet, dass das System die Kosten der zellfreien Proteinsynthesereaktion im Vergleich zum Stand der Technik um 40 % gesenkt hat, während 36,000 experimentelle Bedingungen über sechs iterative Zyklen hinweg durchgeführt wurden.“
Die menschliche Beteiligung beschränkte sich hauptsächlich auf die Reagenzienvorbereitung, das Be- und Entladen sowie die Systemüberwachung, während Versuchsplanung, Durchführung, Datenauswertung und Hypothesenbildung vom GPT-5-gesteuerten autonomen Labor übernommen wurden.
Das verwendete Modell wurde als Open Source veröffentlicht, Die KI-optimierte zellfreie Reaktionsmischung kann von der wissenschaftlichen Gemeinschaft bestellt werden.und machte Gingko so zu einem wichtigen Open-Source-Forschungswerkzeug für Wissenschaftler weltweit.
Ginkgo war auch von der US-Regierung 47 Millionen Dollar zugesprochen für die Entwicklung einer großen Forschungseinrichtung für die Genesis-Mission, ein 32,000 Quadratfuß großes Gelände, bekannt als das Fähigkeit zur mikrobiellen molekularen Phänotypisierung (M2PC)Es wird über 100 automatisierte Analysegeräte beherbergen und soll voraussichtlich bis 2030 für Forscher weltweit voll einsatzfähig sein.
„Das Team wird fortschrittliche KI nutzen, um die Funktion von Proteinen und Stoffwechselwegen zu entschlüsseln, die Datengenerierung und -erfassung zu automatisieren und die experimentellen Systeme und Supercomputer des US-Energieministeriums mit Biotechnologie- und KI-Unternehmen zu integrieren.“
Langfristige Perspektive: Ist Ginkgo endlich profitabel?
Vom Schöpfer des Biofoundry-Geschäftsmodells und einem wichtigen Akteur im Bereich der Biosicherheit erfindet sich Gingko nun neu als führendes Unternehmen in der Automatisierung der biologischen Forschung und als wichtiger Partner in der KI-gestützten F&E-Technologie.
Im Zusammenspiel von Biologie und KI werden viele industrielle Prozesse nach und nach durch umweltfreundlichere, klimaneutrale, ungiftige und kostengünstigere Bioprozessalternativen ersetzt. In dieser Zukunftsvision sind Lebensformen so programmierbar wie Computercode, haben aber einen noch größeren Einfluss auf die reale Welt.
Dies stellt eine enorme Chance für Gingko Bioworks dar, sei es für das Projekt, an dem das Unternehmen bereits arbeitet, oder dafür, dass sein automatisiertes Labordesign langfristig zum Standard für die meisten Forschungsteams wird.
Zusammen mit einer Verbesserung des Geschäftsmodells im Bereich Zelltechnik (mit höheren Lizenzgebühren und faireren Umsatzbeteiligungsverträgen) dürfte dies dazu beitragen, dass Gingko in den kommenden Jahren profitabel wird.
(Mehr über andere Unternehmen im Bereich der synthetischen Biologie können Sie auch in „ lesen.Top 5 der börsennotierten Unternehmen im Bereich der synthetischen Biologie")











