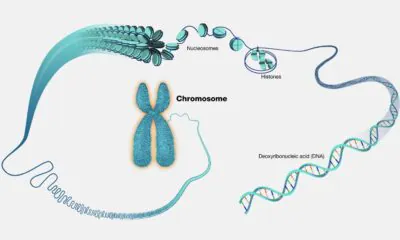
Bioteknologi
CRISPR Therapeutics vs Editas Medicine

Genredigeringens Hype
Genredigering har i en stund vært hyllet som det nye grensefeltet i medisin. Det høyeste entusiasmen blant investorer på dette temaet var tidlig i 2020, med relaterte aksjer som har avtatt siden. Uansett markedssentiment, er genredigering fortsatt en stor sak for medisinske og farmasøytiske selskaper, samt pasienter og leger.
Genredigering er det neste skrittet etter genbehandling. Genbehandling legger til en sunn gen i genomet, men lar den defekte genen være på plass. Redigering, derimot, reparerer den feilaktige genen.
To av de ledende selskapene i sektoren er CRISPR Therapeutics og Editas Medicine.
Hvilken av dem, hvis noen, bør du velge som en investering?
Kort Innføring i CRISPR Genredigering
Mange sykdommer skyldes defekte gener, som fører til ikke-funksjonelle organer eller biokjemiske prosesser. De er ofte svært vanskelige å kurere sykdommer. Infeksjonssykdommer kan løses ved å drepe patogener. Andre problemer kan løses gjennom kirurgi eller legemidler. Men når feilpunktet er i hver celle og krever at kroppen endres på DNA-nivå, er dette mye harder.
I lang tid trodde man at den eneste løsningen var genredigering på tidlig embryo-stadium for å løse problemet når det bare var en celle eller, i beste fall, noen hundre stamceller. Selv da var det vanskelig å sette inn en ny, funksjonell gen i defekte celler, da den tilfeldige innføringen av den nye genen kunne skade andre deler av genomet.
Dette var før CRISPR-Cas9-systemet ble oppdaget. Det kan brukes til å målrette en bestemt plass i genomet. Og deretter gjøre nesten alt molekylærbiologer ønsker, fra å slå ut en gen, helt slette den, eller også redigere den. Det kan også sette inn, på en kontrollert måte, helt nye genetiske sekvenser.

Kilde: CRISPR Therapeutics
Dette endret alt. Tidligere metoder var for grove til å være effektive eller trygge for de fleste pasienter. CRISPR bringer molekylærbiologien til neste nivå, og gjør det mulig å redigere gener på en presis og i-vivo måte.
Forbi CRISPR-Cas9 har forskerne også oppdaget CRISPR-Cas12. Det har litt forskjellige egenskaper som kan vise seg å være bedre i noen tilfeller, som å redigere flere gener på samme tid. Eller for celler som ikke tåler Cas-9 godt.
Mens CRISPR Therapeutics foretrekker Cas9, foretrekker Editas Medicine en versjon av Cas12. Hvis du er teknisk interessert og ønsker å lære mer om forskjellen mellom de 2 CRISPR-systemene, anbefaler jeg å lese denne vitenskapelige publikasjonen og denne artikkelen.
CRISPR Therapeutics’ Teknologi

Selskapet ble grunnlagt i 2013 under navnet Inception Genomics og gikk offentlig i 2016.
En av grunnleggerne av CRISPR Therapeutics er Emmanuel Charpentier, oppdageren av CRISPR-Cas9 og Nobelprisen i kjemi i 2020 for denne oppdagelsen. Så det er trygt å anta at selskapet har et crack-team når det gjelder den vitenskapelige siden av CRISPR-basert genredigering.
Dets teknologi er basert på CRISPR-Cas9, som gjør det mulig å redigere nøyaktig målrettede deler av genomet.
Editas Medicine’s Teknologi

Editas Medicine ble grunnlagt i 2013 og gikk offentlig i 2016. Det startet opprinnelig med å arbeide med Cas9, men fokuserer nå på en proprietær versjon av Cas12 som de har utviklet: AsCas12a.
Vi har dekket i detalj de unike kapasitetene til Cas-12a i en dedikert artikkel. For å resumere det kort:
- Vanlige problemer med Cas9 kunne løses med Cas12a
- Det resulterer i høyere sjanser for genredigering enn med Cas9
- Flere gener kan modificeres på samme tid med Cas12a
CRISPR Therapeutics Pipeline
Blodsykdommer
CRISPR Therapeutics har gjort mest fremgang på 2 sykdommer, Beta-thalassemi og sickle cell sykdom (SCD).
Dette bruker en “ex-vivo”-teknikk: stamceller fra pasientene samles inn, modifiseres/repareres med CRISPR-Cas9 og reintroduceres i kroppen.
Begge er under kliniske prøver i samarbeid med Vertex. I juni 2022, resultatene fra en klinisk prøve viste at 42/44 pasienter med thalassemi var fritt fra behov for blodtransfusjon, med de 2 andre som trengte mye mindre blodtransfusjon.
Ingen alvorlige bivirkninger ble funnet hos SCD-pasienter. To thalassemi-pasienter hadde alvorlige bivirkninger, som har blitt helbredet siden.
Totalt sett ser blodterapien ut til å være en suksess, og sikkerhetsprofilen er akseptabel når man tar hensyn til hvor livstruende og vanskelige å leve med disse sykdommene er. Du kan lære mer om erfaringen til den kurerte pasienten i denne podkasten som intervjuer en av deltakerne i prøven.
Oncologi
En annen anvendelse av CRISPR Therapeutics’ teknologi er kreftbehandling. Ideen er å bruke modifiserte immunceller til å angripe kreftceller. Inntil nå, måtte celler fra pasienten bli genetisk modifisert, noe som tok flere uker, noe som ofte kunne være for sent for en pasients raskt forverrende helse.
I stedet utvikler selskapet en modifisert celle som kan produseres på forhånd og passe alle pasienter. Metoden for å målrette kreftcellen er ikke ny, men muligheten til å starte behandlingen umiddelbart er. Muligheten til å produsere en batch av produkter for hundrevis av pasienter på en gang er også verdifullt, da det kan redusere kompleksiteten og kostnadene til denne terapien.
Selskapet har for øyeblikket 8 kandidater i pipelinen, hvorav 2 allerede er i kliniske prøver.
Diabetes
CRISPR Therapeutics samarbeider også med selskapet ViaCyte for å forbedre deres produkt. ViaCyte har som mål å kurere type-1 diabetes. Dette er en sykdom som rammer 8 millioner mennesker og krever livslang behandling med insulin.
Problemet med ViaCytes nåværende design er at det krever en livslang immunsuppressiv behandling, noe som kommer med sine egne risikoer og problemer. Dette har dramatisk redusert størrelsen på ViaCytes marked.
Med hjelp av CRISPR, ViaCyte har som mål å gjøre sin løsning til en livslang kur for alle type-1 diabetikere.
Løftende er at samme ide kan brukes for mange andre sykdommer hvor en bestemt type celle må erstattes. Dette kan inkludere type-2 diabetes, som rammer mer enn 6% av verdens befolkning, samt hepatitis, cirrhose eller andre degenererende sykdommer.
In-vivo Teknikker
Hver av disse 3 anvendelsene bruker ex-vivo-tilnærmingen til å modifisere celler i laboratorium og reintrodusere dem i pasientene. Dette er ikke mulig for noen sykdommer, for eksempel muskelsykdommer eller lungesykdommer. Derfor prøver CRISPR Therapeutics også å modifisere cellene til pasientene direkte i kroppen, med såkalte “in-vivo”-teknikker. Dette bruker enten virus som vektorer eller mRNA-teknikker ikke ulik mRNA-vaksiner.
Dette målretter en rekke sykdommer, inkludert muskeldystrofi og cystisk fibrose (begge i samarbeid med Regeneron), hemofili (i samarbeid med Bayer) og hjertesykdommer.
På lengre sikt forventer CRISPR Therapeutics at in-vivo-teknologien skal bli deres flaggskip og sentrum for deres kommersielle strategi, “i stand til å løse 90% av de mest utbredte alvorlige monogeniske sykdommene” (se side 35)
Kliniske Prøver
Totalt sett har CRISPR Therapeutics gjort mye fremgang.
Det søker nå om kommersialisering av sine blodterapiprodukter, som kan omfatte så mange som 30 000 pasienter i USA og EU. Godkjenning er aldri en sikker sak, men publiserte data sommeren 2022 indikerer livsforbedrende effektivitet og en akseptabel sikkerhetsprofil. Sannsynligvis kan produktet bli godkjent for alvorlige tilfeller i alle fall. Dette bør være en sterk katalysator for aksjen, da det vil være den første produktgodkjenningen for CRISPR Therapeutics.
Ytterligere forbedring kan øke markedet til 166 000 pasienter, eller selv 450 000 hvis in-vivo-metoden viser seg å være suksessfull (se den lenkede presentasjonen side 8).
Kreftbehandlingsprøvene er fortsatt i tidlige faser, så det er umulig å forutsi utfallet. Preliminære data har vært oppmuntrende.
Diabetestreatmentene gikk inn i prøve 2nd februar 2022. Så det er for tidlig å dømme det, men resultater fra denne prøven kan være en annen sterk katalysator for aksjen i 2023.
Editas Medicine Pipeline

Øyesykdom
Editas Medicine arbeidet tidligere med å kurere blindhet på grunn av Leber congenital amaurosis 10, gjennom sin EDIT-101-behandling. Fase 1/2 klinisk prøve gikk bra, og viste bevis for konseptet.
Imidlertid ser Editas nå på å lisensiere ut sin teknologi for denne sykdommen og fokusere eksklusivt på sin egen blodsykdomsbehandling. Det ser ut til at den strategiske omorienteringen skyldes:
- Denne behandlingen var avhengig av Cas9-metoden, noe selskapet ikke er interessert i å bruke fremover.
- Dette etterlater den eksisterende pipelinen til å avhenge eksklusivt av AsCas12a, som ikke er underlagt noen tvist om patenter og IP, i motsetning til Cas9-teknologier.
- Dette er en svært nisjet anvendelse, med bare 1 500 relevante pasienter i USA.
Blodsykdom
Editas fokuserer nå på Sickle Cell Disease (SCD), og går dermed inn i direkte konkurranse med CRISPR Therapeutics’ egen genredigeringsbehandling for SCD.
Editas’ strategi er å bruke det konstruerte AsCas12a CRISPR-systemet, som leverer en overlegen redigerings-effektivitet og spesifisitet enn konkurrentenes system som bruker Cas9.
Selskapet bruker AsCas12a til å aktivere genene for fosterhemoglobin hos voksne, og produserer funksjonelt fosterhemoglobin for å erstatte det som ikke fungerer i tilfeller av SCD.

Andre mål
Selskapet har også programmer i tidlige faser i onkologi (kreft) i samarbeid med BMS og Immatics. Andre organer blir også forsket, sannsynligvis for in-vivo-terapier. Lite er blitt avdekket om disse programmene så langt.
Kliniske Prøver
Den initielle prøven for SCD-behandling på 2 pasienter viste en god sikkerhetsprofil i resultater publisert i desember 2022. De initielle resultater viser også bevis for konseptet av behandlingen, med en betydelig økning av hemoglobinnivåene i pasientens blod og reduksjon eller fjerning av sykdommens symptomer. Data fra flere pasienter skal publiseres i midten av 2023.
Neste skritt er å inkludere 40 pasienter i en klinisk prøve i fase 1/2, med de første resultater forventet ved slutten av 2023.
Finanser og Verdi
1. CRISPR Therapeutics
CRISPR Therapeutics’ verdi i begynnelsen av 2023 har sunket betydelig fra et høydepunkt på 13,7 milliarder dollar i januar 2021.
(CRSP
)
(CRSP )
Ettersom selskapet ikke har et kommersielt produkt ennå, avhenger det av sin kontantbeholdning og avtaler med større farmasøytiske selskaper.
For eksempel, registrerte det 912 millioner dollar i inntekt fra samarbeidet med Vertex i 2021. Dette kan sammenlignes med 438 millioner dollar i FoU-utgifter og 102 millioner dollar i administrative utgifter i samme år. Med bare 500 ansatte, ser selskapet ut til å være ganske lean, effektivt og fokusert på innovasjon.
Selskapet har omtrent 2 milliarder dollar i kontanter, noe som bør dekke selskapets behov frem til 2024. Det har ingen betydelige gjeld eller forpliktelser utover nåværende operative forpliktelser og leieavtaler for sine produksjonsanlegg.
Totalt sett ser selskapets finanser solide ut, selv om det kanskje må samle inn mer penger på et tidspunkt hvis sine sykdoms- og thalassemi-legemidler ikke raskt blir godkjent. I denne sammenhengen burde den høyere aksjeprisen i 2021 ha blitt bedre utnyttet til å samle inn midler enn å risikere den nåværende lavere verdien.
2. Editas Medicine
Liksom de fleste biotekniske selskaper, er Editas Medicines verdi ganske lavere enn sitt høydepunkt på 5,6 milliarder dollar i januar 2021.
(EDIT )
Med hensyn til modenheten av sin pipeline, er Editas bare nå i ferd med å lansere 40+ pasientprøver som CRISPR Therapeutics allerede har fullført. Så det er sannsynlig at det ligger 1-2 år bak når det gjelder mulig kommersialisering.
Selskapet hadde et tap på 193 millioner dollar i 2021, hvorav 142 millioner dollar ble brukt på FoU. Ettersom det nå har 507 millioner dollar i løpende midler, er likviditeten tilstrekkelig for hele 2023, selv når man tar hensyn til den ekstra kostnaden for den kommende kliniske prøven.
Editas Medicine kan trenge ekstra finansiering før det når kommersialisering, men dette vil sannsynligvis ikke være årsaken til en alvorlig utvanning av aksjonærer, takket være den solide nåværende kontantbeholdningen. Det utstedte aksjer verdt 203 millioner dollar i 2020 og 249 millioner dollar i 2021, og gjorde god bruk av den daværende høyere aksjeprisen.
Totalt sett er Editas Medicine på et tidligere stadium enn CRISPR Therapeutics. Men takket være sin fokuserte tilnærming sentrert rundt bare en behandling og en sykdom, har det en lignende risikoprofil når det gjelder kontantbeholdning og risiko for utvanning.
Hvilken en skal velge?
CRISPR Therapeutics er sektorens leder, og nyter godt av sin først-be-til-å-oppdage-fordel, ettersom det ble grunnlagt av oppdageren av Cas9-teknologien. Det har også en mye bredere portefølje, som dekker SCD og andre blodsykdommer, kreft og til og med diabetes. Så det totale potensielle markedet er mye bredere.
Det er også mer avansert i sine kliniske prøver, og har en realistisk sjanse til å se minst ett produkt kommersialisert innen 12-24 måneder.
Hvor CRISPR Therapeutics kanskje mangler, er i sin avhengighet av Cas9-teknologien, som kan være litt mindre effektiv på lengre sikt. Det er vanskelig å bedømme om disse tekniske forskjellene vil resultere i praktiske forskjeller i terapeutisk effektivitet.
Editas Medicine er en pionér i å gjøre Cas12a til et praktisk medisinsk verktøy. Ved å konsentrere sine anstrengelser om SCD, går det direkte i konkurranse med CRISPR Therapeutics’ egen SCD-behandling. Så mye av fremtidens suksess eller fiasko for Editas vil avhenge av om dens behandling for SCD viser seg å være overlegen CRISPR Therapeutics’.
Begge selskapenes verdier kan regnes som omtrent like, ettersom CRISPR Therapeutics har en mye høyere verdi og en mye mer diversifisert pipeline, spesielt siden begge har en lignende risikoprofil med en stor kontantbeholdning som dekker de neste 1-2 års utgifter.
Det er også mulig at begge selskapene vil nå kommersialisering og dele SCD-markedet på relativt like vilkår.
For investorer som ser etter et svært innovativt og fokusert selskap, kan Editas Medicine være et foretrukket valg.
For investorer som ser etter en mer spredt FoU-risiko, bør CRISPR Therapeutics’ bredere pipeline være mer beroligende. Upsiden i 4-6 års tidsramme for CRISPR Therapeutics kan også være større, takket være dens innsats i det svært store markedet for diabetes.